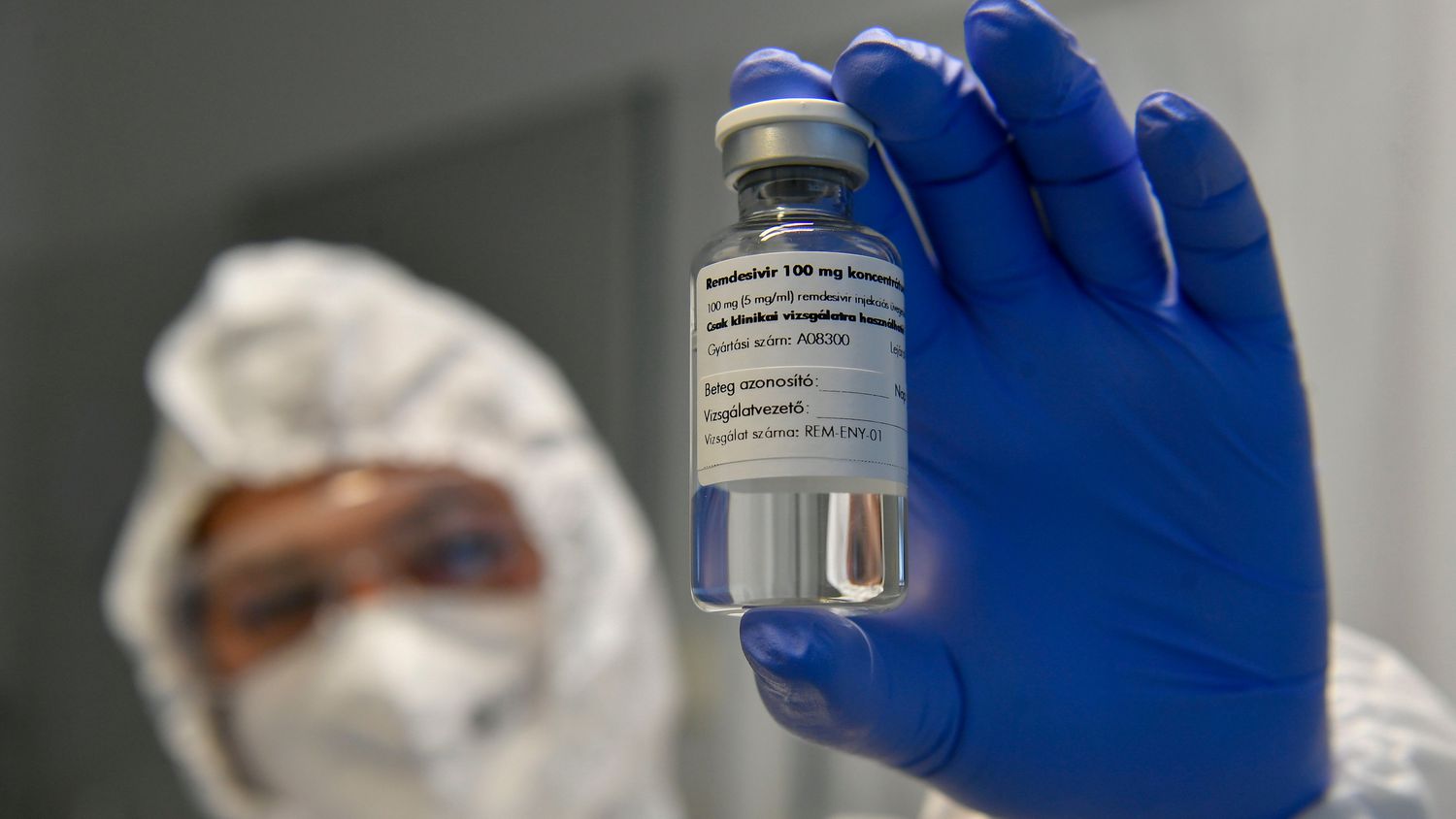
Los laboratorios Gilead Sciences recibieron este jueves la aprobación completa del antivirual Remdesivir como tratamiento contra el COVID-19 por parte de la Administración de Alimentos y Medicamentos de Estados Unidos (FDA, por sus siglas en inglés). Se trata del primer y único fármaco totalmente aprobado por la FDA para tratar a pacientes con coronavirus.
En el mes de mayo, la FDA había emitido una autorización de uso de emergencia de la droga, después de que se descubriera que el tratamiento acortaba el tiempo de recuperación de algunos pacientes hospitalizados. La decisión llegaba dos días después de que Gilead, el laboratorio que produce el antiviral, publicara un estudio preliminar sobre su eficacia en pacientes que habían contraído la enfermedad.
Sin embargo, la Organización Mundial de la Salud (OMS) advirtió la semana pasada que un ensayo global de terapias contra el coronavirus determinó que el medicamento no tiene un efecto sustancial en la reducción de los días hospitalizados ni en las posibilidades de supervivencia en los casos más graves del virus. Los resultados se desprendieron del muy esperado ensayo Solidarity, que estudió los efectos del Remdesivir y otros tres posibles fármacos en 11.266 pacientes hospitalizados a nivel gobal.
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/ABGKPAQ3MQMRHUJEXJUEV5S6OY.jpg) El Remdesivir es un profármaco antiviral que pertenece a la familia de los análogos de los nucleótidos y actúa inhibiendo una enzima del virus indispensable para su multiplicación (REUTERS)
El Remdesivir es un profármaco antiviral que pertenece a la familia de los análogos de los nucleótidos y actúa inhibiendo una enzima del virus indispensable para su multiplicación (REUTERS)El Remdesivir es un profármaco (una sustancia inocua que se transforma en fármaco dentro del organismo cuando es metabolizada) antiviral. Pertenece a la familia de los análogos de los nucleótidos y actúa inhibiendo una enzima del virus indispensable para su multiplicación.
Comenzó como un tratamiento para el ébola y el virus de Marburgo, pero también demostró utilidad contra el virus respiratorio sincitial, el de Junín, el de la fiebre de Lassa y algunos coronavirus como los causantes del síndrome respiratorio de Medio Oriente (MERS) y del síndrome respiratorio agudo grave (SARS). Actualmente se estudia su uso contra los virus de Nipah, Hendra y el COVID-19. En pocas palabras, su mecanismo consiste en interferir la replicación del microorganismo invasor.
Un informe publicado el 8 de octubre en la revista New England Journal of Medicine confirmó los beneficios del Remdesivir para tratar a las personas hospitalizadas por COVID-19. En él, los investigadores dirigidos por un equipo del Instituto Nacional de Alergias y Enfermedades Infecciosas (NIAID) proporcionaron los datos finales de un estudio que publicaron por primera vez en mayo.
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/BOXTB6PQJJHKREFGHVU2WRDZNQ.jpg) “Estos datos refuerzan el valor del Remdesivir en pacientes hospitalizados” (REUTERS)
“Estos datos refuerzan el valor del Remdesivir en pacientes hospitalizados” (REUTERS)Todos los participantes mostraron evidencia de infección respiratoria, principalmente neumonía, y se consideró que el 85% tenía una enfermedad grave, lo que significaba que tenían al menos uno de tres síntomas: sus niveles de oxígeno en sangre estaban por debajo del 94%; requerían oxígeno suplementario; o necesitaban un ventilador para respirar.
“Estos datos refuerzan el valor del Remdesivir en pacientes hospitalizados”, dijo el médico John Beigel, director asociado de investigación clínica en la división de microbiología y enfermedades infecciosas del NIAID, citado por el Times.
:quality(85)/cloudfront-us-east-1.images.arcpublishing.com/infobae/U2NFG2FED5AWHKRVFYG5ZI3FZ4.jpg) Aunque se ha demostrado inicialmente su eficacia en pacientes graves o muy graves, su perfil de seguridad no está totalmente esclarecido (Europa Press)
Aunque se ha demostrado inicialmente su eficacia en pacientes graves o muy graves, su perfil de seguridad no está totalmente esclarecido (Europa Press)Además, el Remdesivir presenta algunas similitudes estructurales y funcionales con otro medicamento antiviral, el tenofovir, que ha confirmado ser nefrotóxico, tanto en pacientes con hepatitis crónica tipo B como en modelos animales. En humanos, el Remdesivir se elimina en gran medida a nivel renal, lo que podría ocasionar una acumulación orgánica del medicamento en aquellos pacientes con insuficiencia renal. También se han informado efectos adversos gastrointestinales de menor intensidad, como náuseas y diarrea, en un 3% a 5% de los pacientes tratados, aunque estos efectos podrían asociarse a la sintomatología de la COVID-19.
Fuente: INFOBAE